Erstellen Sie die rechtskonforme Einweisungsdokumentation und erfüllen Sie die Dokumentationspflicht bei medizintechnischen Geräten nach MPDG und MPBetreibV.

Erstellen Sie die rechtskonforme Einweisungsdokumentation und erfüllen Sie die Dokumentationspflicht bei medizintechnischen Geräten nach MPDG und MPBetreibV.
Seit dem 1. Januar 2017 nimmt der Gesetzgeber Betreiber von Medizinprodukten noch stärker in die Pflicht. Viele Krankenhäuser und medizinische Einrichtungen werden durch die überarbeiteten Anforderungen vor nahezu unlösbare Aufgaben gestellt. Hunderte Anwender müssen in Unmengen von Medizinprodukten eingewiesen werden, was in einem unfassbaren Dokumentationsaufwand resultiert. Permanente Veränderungen wie Personalwechsel, Umzüge oder Firmware-Updates von Medizinprodukten machen eine rechtskonforme Dokumentation auf Papier oder in Tabellenkalkulationsprogrammen – im Hinblick auf Aktualität, Aufwand und Sicherheit – schlichtweg unmöglich. MED-INSTRUCTION ermöglicht Betreibern und Anwendern von Medizinprodukten durch viele Softwareautomatismen und eine Verknüpfung zur Medizintechnikverwaltung MED einen einzigartigen Weg aus dem Dokumentationsdilemma.
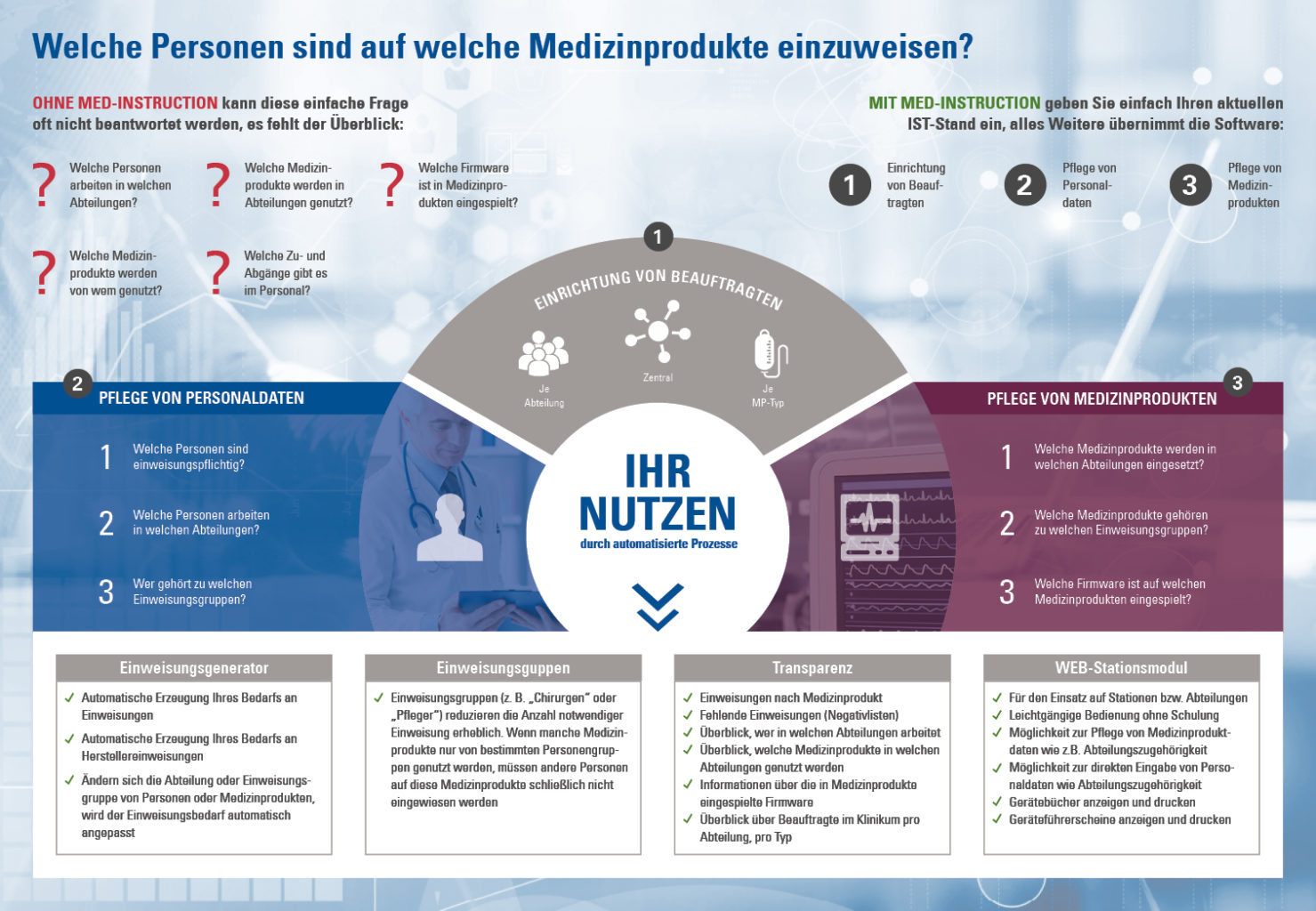
Betreiber von einweisungspflichtigen Medizinprodukten müssen nicht immer Krankenhäuser sein. Auch Unternehmen und andere Einrichtungen, die Medzinitechnikprodukte zur Verfügung stellen, können als Betreiber von medizintechnischen Geräten unter die Einweisungspflicht fallen. Das geht aus der Neufassung der MPBetreibV hervor, welche seit dem 1. Januar 2017 genauer abgegrenzt, wer als Betreiber gilt.
Wer Medizinprodukte betreiben oder anwenden möchte, muss nach § 4 Abs. 2 MPBetreibV eine dafür erforderliche Ausbildung besitzen oder über die notwendigen Kenntnisse bzw. Erfahrungen verfügen. Nach § 4 Abs. 3 MPBetreibV ist dazu eine Einweisung in die ordnungsgemäße Handhabung notwendig. Dieser Abschnitt regelt auch Ausnahmen, in welchen Medizinprodukte nicht unter die Einweisungspflicht fallen. Welche Medizingeräte davon betroffen sind, wird in Anlage 1 der MPBetreibV geregelt.
§ 7 Abs. 1 MPBetreibV beschäftigt sich mit der Instandhaltung von Medizinprodukten, insbesondere von Instandhaltungsmaßnahmen sowie der Instandsetzung. „Die Instandsetzung umfasst insbesondere die Reparatur zur Wiederherstellung der Funktionsfähigkeit“ [§ 7 Abs. 1 MPBetreibV] von medizintechnischen Geräten und Medizinprodukten. § 7 Abs. 2 MPBetreibV legt fest, dass der Betreiber nur Personen, Betriebe oder Einrichtungen beauftragen darf, welche die Voraussetzungen nach § 5 MPBetreibV erfüllen.
Das einzigartige modulare Konzept von waveware® ermöglicht es, beliebige Softwarepakete in einer Installation zu verknüpfen und somit ineinander verzahnte Softwareprozesse zu realisieren. So ist es möglich, das Einweisungspaket MED-INSTRUCTION mit der Medizintechnikverwaltung (MED) zu verbinden. Dieses stellt eine MPDG-konforme Verwaltung Ihrer Medizingeräte sicher und unterstützt Sie ebenfalls bei der Beauftragung von Wartungen und Kontrollen wie der systemtechnischen (STK) oder messtechnischen Kontrolle (MTK).
Regelungen zu den sicherheitstechnischen und messtechnischen Kontrollen sind in § 11 MPBetreibV (STK) bzw. § 14 MPBetreibV (MTK) genauer definiert.
§ 10 Abs. 1 Nr. 2 MPBetreibV legt fest, dass ein medizintechnisches Gerät nur betrieben und angewendet werden darf, wenn zuvor eine sachgerechte Einweisung in die Handhabung, Anwendung und den Betrieb des Medizinprodukts durch den Hersteller oder eine vom Hersteller beauftragte Person erfolgt ist. Dabei ist eine Verbindung zu anderen Medizinprodukten, Gegenständen und Zubehör zu berücksichtigen. Eine Einweisung für ein baugleiches medizinisches Gerät, für welches bereits eine Einweisung existiert, ist hingegen nicht notwendig. Eine eindeutige Dokumentations- und Nachweispflicht wird durch § 10 Abs. 3 MPBetreibV definiert.
Die Anwendung MED-INSTRUCTION beinhaltet ein ausgeklügeltes Beauftragten-Management. Dieses unterstützt den Betreiber beim Anlegen von Herstellereinweisungen. Jene befähigen einen im Unternehmen beauftragten Mitarbeiter, künftig Geräte-Einweisungen für bestimmte Medizintechnikprodukte durchzuführen. Die Software verwaltet alle Beauftragten mit ihren zuständigen Abteilungen bzw. Medizinprodukt-Typen. Bei der Einweisung von Personal durch die vom Hersteller beauftragten Mitarbeiter wird durch MED-INSTRUCTION zudem eine rechtskonforme Dokumentation sichergestellt.
Das Gesetzt gibt vor, dass ein Betreiber für sämtliche Medizinprodukte der Anlagen 1 und 2 ein Medizinproduktebuch zu führen hat. Der Gesetzgeber überlässt nach § 12 Abs. 2 MPBetreibV dem Betreiber, welchen Datenträger er dafür nutzt. In vielen Einrichtungen werden Medizinproduktebücher noch handschriftlich oder mit einem Tabellenkalkulationsprogramm geführt. Diese beiden Methoden besitzen jedoch – im Hinblick auf ständige Veränderungen und mangelnde Auswertungsmöglichkeiten – gravierende Schwächen. Hinzu kommt, dass einem Anwender während der Arbeitszeit Zugang zum Medizinproduktebuch gewährt werden muss. Dies ist oftmals mit großen organisatorischen Anstrengungen und einer tiefgehenden Fachkenntnis verbunden, um die Datenverwaltung zu verstehen. Aus diesem Grund existieren in vielen Einrichtungen und Unternehmen große rechtliche Gefahrenstellen. Durch die Neufassung der MPBetreibV werden die gesetzlichen Vorschriften nochmals verdeutlicht.
Die Anwendung MED (Medizintechnikverwaltung) kann genauso wie MED-INSTRUCTION modular in wave Facilities hinzugebucht werden. Mit der Medizintechnikverwaltung können beliebige Medizinprodukte und medizintechnische Geräte gemäß den Richtlinien des Medizinprodukterecht-Durchführungsgesetzes (MPDG) und der Medizinprodukte-Betreiberverantwortung (MPBetreibV) verwaltet werden. Dazu gehört das vollständige Erfassen unter Berücksichtigung der verschiedenen Risikoklassen. Darüber hinaus liefert die Anwendung durch umfangreiche Auswertungsfunktionen die optimale Datenbasis für wichtige wirtschaftliche Entscheidungen. Zur Sicherstellung der elektrischen Sicherheit nach DGUV V3, BetrSichV und VDE bietet sich die Schnittstelle SAFETY TESTERS zu zahlreichen Prüfgeräten an. Etwa 1.200 Krankenhäuser in ganz Deutschland vertrauen auf die Software von Loy & Hutz.
MEDFür alle nicht implementierbaren Medizinprodukte der jeweiligen Betriebsstätte muss ein Bestandsverzeichnis geführt werden. Mit der Anwendung MED (Medizintechnikverwaltung) erfassen Sie alle medizintechnischen Geräte mit allen erforderlichen und individuell gewünschten Angaben. Sämtliche Medizinprodukt-Stammdaten werden an zentraler Stelle geführt. Somit erfüllen Sie alle Anforderungen nach §§ 12, 13 MPBetreibV mit derselben Software. Damit entfällt eine unwirtschaftliche und doppelte Datenhaltung, welche auch vom Gesetzgeber gestattet wird, denn “die Aufnahme in ein Verzeichnis, das auf Grund anderer Vorschriften (z.B. § 12 MPBetreibV) geführt wird, ist zulässig”. Weiterhin können Sie Medizinprodukte und medizintechnische Geräte durch das Hinzubuchen zusätzlicher Softwarepakete – beispielsweise durch FM-BASIS – an einem beliebigen Standort verorten. Damit haben Sie nicht nur einen alphanumerischen Hinweis, wo sich das jeweilige Medizinprodukt befindet, sondern können auch detaillierte Auswertungen und Prozesse (z.B. Umzugsplanung) automatisieren.
Basis für erfolgreiches Einweisungsmanagement nach der MPBetreibV ist die Festlegung von Beauftragten. Zuständigkeiten und Zuordnungen von Beauftragten werden in MED-INSTRUCTION über sogenannte Beauftragungsbereiche definiert. Nach der Konfiguration eines Beauftragungsbereichs können die Beauftragten zugeteilt werden. Das Einweisungspaket MED-INSTRUCTION verfügt über ein integriertes Beauftragten-Management und nimmt Ihnen durch automatisierte Softwareprozesse den Großteil Ihrer Arbeit ab: Nach dem Anlegen von Beauftragten und Beauftragungsbereichen sehen Sie sofort, welche Beauftragten über eine Befugnis für Einweisungen verfügen und in wessen Zuständigkeitsbereich die gewünschte Einweisung fällt. Sie erfahren ebenfalls, welche Herstellereinweisungen noch fehlen.
Mit MED-INSTRUCTION richten Sie schnell und einfach Beauftragungsbereiche ein und weisen diesen Beauftragten zu. Sie können folgende Beauftragungsbereiche einrichten:
In Abhängigkeit der Unternehmensgröße kann so frei definiert werden, ob eine Person für Einweisungen im gesamten Unternehmen zuständig ist oder sich mehrere Beauftragte die Durchführung von Einweisungen in Bereiche aufteilen. Hierbei können beauftragte Personen zu verschiedenen Medizintechnik-Typen und/oder einem Bereich (z.B. Abteilung) zugeordnet werden. Natürlich sind auch Mischformen und Stellvertreterregelungen möglich. Damit Beauftragte ihre Mitarbeiter auf einen bestimmten Medizinproduktetyp einweisen können, benötigen sie eine Herstellereinweisung.
Aus Beauftragungsbereichen und Beauftragten ermittelt MED-INSTRUCTION vollautomatisiert den Bedarf an Herstellereinweisungen und zeigt diesen in einer übersichtlichen Liste auf. Parallel dokumentiert das System, welcher Bedarf an Herstellereinweisung besteht und welche Person zu welchem Zeitpunkt eingewiesen wurde.
Bei jedem Medizinprodukt trägt MED-INSTRUCTION automatisiert den zuständigen Beauftragten ein. Damit kann an jedem Medizinprodukt die zuständige Ansprechperson sofort ermittelt werden. Fehlt dieser Wert bei einem Medizinprodukt, wurde im Beauftragungsbereich noch kein Beauftragter zugeordnet.
Wird in waveware® ein neuer Stammdatensatz eines Medizinprodukts angelegt, ermittelt das System automatisiert den geeignetsten Einweisungsbeauftragten im Unternehmen. In den Softwarealgorithmus fließen Produkttyp, Bereichszuständigkeit, Rangfolge sowie Stellvertreterregelungen ein. Es wird sichergestellt, dass der ermittelte Einweisungsbeauftragte eine Befugnis mit aktueller Gültigkeit besitzt. Fehlen die erforderlichen Qualifikationen, legt das System automatisiert eine durchzuführende Herstellereinweisung an. Mit einem Klick wird eine Liste mit allen beauftragten, noch nicht durchgeführten Herstellereinweisungen erzeugt.
Bisher müssen Beauftragte überblicken, wer auf welcher Station arbeitet, welche Geräte auf welcher Station genutzt werden, mit welcher Firmware ein Medizinprodukt aktuell ausgestattet ist und welche Produkttypen von welchen Personalgruppen genutzt werden dürfen. Aus all diesen Informationen müssen Beauftragte anschließend den Einweisungsbedarf ableiten. Unter wirtschaftlichen Gesichtspunkten ist ein normgerechtes Einweisungsmanagement aufgrund ständiger Personalwechsel, abteilungsübergreifender Zusammenarbeit und weiterer Veränderungen nahezu unmöglich. MED-INSTRUCTION vereinfacht Ihren Aufwand erheblich: Sie geben an, welche Personen in welchen Abteilungen arbeiten und welche Geräte auf welcher Station zum Einsatz kommen. Der Einweisungsgenerator greift auf Stammdaten zu, prüft systematisch Zuordnungen und legt automatisiert alle erforderlichen Einweisungsbedarfe an.
In Krankenhäusern und medizinischen Einrichtungen gibt es meistens mehrere hundert Medizinprodukte und eine oftmals ebenso große Anzahl von beschäftigten Personen wie Fachärzte, Chirurgen, OP-Personal, Krankenschwestern, Krankenpfleger etc. Daraus ergeben sich tausende potentielle Einweisungen, die nach der Neufassung der Medizinprodukte-Betreiberverordnung (MPBetreibV) vom 01.01.2017 nachweisbar dokumentiert werden müssen. Oftmals fehlt dem verantwortlichen Personal jedoch der Überblick, welche Personen welche Geräte verwenden und wo die entsprechenden Einweisungen dokumentiert wurden. Da die Dokumentation oftmals noch auf Papier oder in Excel erfolgt, ist eine effiziente Suche oder Auswertung im erforderlichen Ausmaß nicht möglich. Es ist keine Seltenheit, dass Medizinprodukte abteilungsübergreifend genutzt werden oder Personen gleich mehreren Abteilungen angehören (z.B. als Springer). Hinzu kommen permanent wechselnde Herausforderungen wie Personalwechsel, Umzüge oder Firmware-Updates von Medizinprodukten. All dies beeinflusst die Einweisungsdokumentation. Mit bisherigen Mitteln kann dieser organisatorische Aufwand wirtschaftlich nicht geleistet werden.
Mit der Anwendung MED-INSTRUCTION gelingt es, der Überforderung durch gesetzliche Auflagen Herr zu werden. Die moderne und übersichtliche Oberfläche sorgt dafür, dass die Erstellung einer Einweisung leichtgängig, effizient und ohne Expertenkenntnisse durchgeführt werden kann. Zunächst werden Personal- und Medizinproduktestammdaten im System erfasst. Zuordnungen geben Aufschluss, wo sich beispielsweise ein Medizintechnikprodukt befindet oder in welcher Abteilung eine Person arbeitet. Der integrierte Einweisungsgenerator prüft anschließend automatisiert, ob eine Person einweisungspflichtig ist und gleichzeitig ein einweisungspflichtiges Gerät in der Abteilung dieser Person steht. Werden diese beiden und weitere Kriterien gemäß MPBetreibV erfüllt, legt der Einweisungsgenerator eine durchzuführende, offene Einweisung an. Wechselt eine Person die Abteilung, prüft der Generator, ob es dort neue Medizinprodukte gibt und legt im positiven Fall ebenfalls automatisch neue Einweisungsbedarfe an. Auch wenn ein medizintechnisches Gerät ein Firmware-Update erhält, prüft eine Software-Routine des Einweisungsgenerators, ob eine neue Einweisung für die betroffenen Personen angelegt werden muss.
Müsste in einer medizinischen Einrichtung jede Person auf jedes Medizinprodukt eingewiesen werden, entstünde ein immenser Einweisungsbedarf. Mit den Einweisungsgruppen in MED-INSTRUCTION reduzieren Sie Einweisungsbedarfe auf das erforderliche Maß. Die Einweisungsgruppen lassen sich mit der Anwendung MED-INSTRUCTION leicht einrichten. Anschließend lässt sich Personal einer Einweisungsgruppe (z.B. “Pflegekräfte”) zuordnen. Medizintechnische Geräte und Medizinprodukte können ebenfalls die Einweisungsgruppe “Pflegekräfte” zugewiesen bekommen. Für diese Gerätetypen werden nur Einweisungsbedarfe für Mitarbeiter mit identischer Einweisungsgruppe erstellt. Die Anwendung MED-INSTRUCTION dokumentiert detailliert alle durchgeführten Aktionen und kann jederzeit ausgelesen werden.
In der täglichen Praxis müssen einweisungsrelevante Informationen auch von ungeschultem Personal angelegt und abgerufen werden. Zusammen mit dem Anwendungs-Client waveware® NETPROCESS bietet MED-INSTRUCTION ein WEB-Stationsmodul, mit welchem sich wichtige Fragen (“Wer ist Beauftragter für dieses Medizinprodukt?”; “Welche Einweisungen fehlen?”) schnell klären lassen. Das WEB-Stationsmodul zeigt erstellte Einweisungsbedarfe auf der übersichtlichen Weboberfläche an, aus welchen in wenigen Schritten Medizinprodukte-Einweisungen erstellt und dokumentiert werden. Über den waveware® NETPROCESS-Client ermöglicht das WEB-Stationsmodul, Personal, Medizinprodukte und Zuordnungen direkt vor Ort zu pflegen. Anwender finden sich auch ohne Schulung sofort auf der Softwareoberfläche zurecht.
Die Hauptfunktion stellt die einfache Erfassung und Dokumentation von Medizinprodukte-Einweisungen auf einer leicht bedienbaren Web-Oberfläche dar. Diese stellt gleichzeitig viele Auswertungen und Listen zur Verfügung, worüber sich zentrale Fragen rund um Einweisungen beantworten lassen. Wer ist Teil der Abteilung? Wer ist einweisungspflichtig? Welche offenen Einweisungsbedarfe gibt es? Weiterhin kann die Software zur Ausstellung eines Geräteführerscheins, welcher die bereits erhaltenen Einweisungen einer Person (z.B. für den Wechsel in ein anderes Krankenhaus) ausweist, herangezogen werden. Auch die Erstellung eines Einweisungs-Laufzettels ist möglich. Damit weiß ein Mitarbeiter, welche Einweisungen er persönlich noch durchführen muss, bevor er ein entsprechendes Medizinprodukt anwenden darf.
Die webbasierte Plattform waveware® NETPROCESS verbindet die Nutzung leistungsstarker Funktionen der CAFM-Software wave Facilites mit dem Komfort einer übersichtlichen und webbasierten Eingabemaske. Die ASP.NET-Oberfläche als Ergänzung zur Standardinstallation von waveware® bringt eine komplett neue und überarbeitete Benutzeroberfläche mit sich. Neben dem Design wurde ebenfalls ein leichtgängigeres Benutzerkonzept umgesetzt, welches die Eingabe und Verwaltung von Einweisungen nochmals deutlich verbessert. Die in waveware® NETPROCESS angebotenen Funktionen können standortunabhängig von beliebig vielen Anwendern gleichzeitig genutzt werden. Die Vorteile sind enorm: Eine einfache und unkomplizierte Dateneingabe sowie ein schnelles Abrufen von Informationen auf einer modernen Web-Oberfläche spart Zeit und Geld. Die Schnittstelle zur Datenbank ermöglicht zudem viele Hintergrundabfragen, Statusanzeigen und umfangreiche Katalogfunktionen.
Die Einweisung selbst wird am betriebsbereiten, fertig aufgestellten Gerät durchgeführt. Inhalte der Einweisung sind die Bedienung des Geräts und das Zusammenspiel des Geräts mit eventuell vorhandenem Zubehör. Neben der Verwendung des Betriebshandbuchs sind auch sämtliche Sicherheitshinweise und Zusatzbestimmungen ein wichtiger Bestandteil der Einweisung. Welche medizintechnischen Geräte eine Einweisung durch eine befugte Person erfordern, wird in der Anlage 1 der MPBetreibV geregelt. Die technischen Inhalte einer Einweisung sind abhängig von der Art des jeweiligen Geräts. Eine Einweisung, die nicht oder nur mangelhaft dokumentiert wurde, wird vom Gesetzgeber als “nicht stattgefunden” betrachtet. Nachfolgend finden Sie einen Auszug der Liste von Medizinprodukten aus Anlage 1 MPBetreibV.
Mit den in waveware® integrierten Systemfunktionen DMS (Dokumentenmanagement) und ANALYSIS (Auswertung & Analyse) können Sie alle durchgeführten und offenen Einweisungen gesetzeskonform dokumentieren und jederzeit kontrollieren. Ein ausgefülltes und unterschriebenes Einweisungsformular wird dazu eingescannt und per DMS direkt an den Personaldatensatz und/oder an ein medizintechnisches Gerät angehängt. Dashboards und Listen zeigen durchgeführte und noch offene Einweisungen an. Betreiber können so sichergehen, dass keine Einweisung vergessen wurde.
Mit dem Softwarepaket MED-INSTRUCTION von waveware® profitieren Sie beim Dokumentieren von Geräteeinweisungen gleich doppelt. Sämtliche Einweisungsdaten werden nicht nur als Einweisungsprotokoll ausgegeben, sondern auch in der Datenbank abgespeichert. Dort können Sie zu jeder Zeit umfangreiche Auswertungen zu eingewiesenen Personen und Geräten vornehmen. Die unterschriebenen Originaldokumente, wie z.B. das Einweisungsprotokoll, können im integrierten DMS (Dokumentenmanagement) direkt an das jeweilige medizintechnische Gerät angefügt werden.
Nach § 4 Abs. 2 f. MPBetreibV dürfen Medizinprodukte nur von Personen errichtet, betrieben, angewendet und in Stand gehalten werden, die dafür die erforderliche Ausbildung oder Kenntnis und Erfahrung besitzen. Voraussetzung dafür ist die Einweisung durch eine beauftragte Person nach § 4 Abs. 5 MPBetreibV hinsichtlich der sachgerechten Handhabung, Anwendung und des Betriebs des Medizinprodukts. Betreiber müssen nachweisen können, dass sowohl das Personal als auch externe Dienstleister für alle notwendigen Geräte eine Einweisung erhalten haben. Dafür benötigt es eine detaillierte Dokumentation der Einweisung, z.B. in Form eines Einweisungsprotokolls.
[Stand: 24.04.2024]
§ 2 Begriffsbestimmungen
[…]
(2) Betreiber eines Medizinproduktes ist jede natürliche oder juristische Person, die für den Betrieb der Gesundheitseinrichtung verantwortlich ist, in der das Medizinprodukt durch dessen Beschäftigte betrieben oder angewendet wird. Abweichend von Satz 1 ist Betreiber eines Medizinproduktes, das im Besitz eines Angehörigen der Heilberufe oder des Heilgewerbes ist und von diesem zur Verwendung in eine Gesundheitseinrichtung mitgebracht wird, der betreffende Angehörige des Heilberufs oder des Heilgewerbes. Als Betreiber gilt auch, wer außerhalb von Gesundheitseinrichtungen in seinem Betrieb oder seiner Einrichtung oder im öffentlichen Raum Medizinprodukte zur Anwendung bereithält.
(3) Anwender ist, wer ein Medizinprodukt im Anwendungsbereich dieser Verordnung am Patienten einsetzt.
(4) Gesundheitseinrichtung im Sinne dieser Verordnung ist jede Einrichtung, Stelle oder Institution, einschließlich Rehabilitations- und Pflegeeinrichtungen, in der Medizinprodukte durch medizinisches Personal, Personen der Pflegeberufe oder sonstige dazu befugte Personen berufsmäßig betrieben oder angewendet werden.
§ 4 Allgemeine Anforderungen
(1) Medizinprodukte dürfen nur ihrer Zweckbestimmung entsprechend und nach den Vorschriften dieser Verordnung sowie den allgemein anerkannten Regeln der Technik betrieben und angewendet werden.
(2) Medizinprodukte dürfen nur von Personen betrieben oder angewendet werden, die die dafür erforderliche Ausbildung oder Kenntnis und Erfahrung besitzen.
(3) Eine Einweisung in die ordnungsgemäße Handhabung des Medizinproduktes ist erforderlich. Abweichend von Satz 1 ist eine Einweisung nicht erforderlich, wenn das Medizinprodukt selbsterklärend ist oder eine Einweisung bereits in ein baugleiches Medizinprodukt erfolgt ist. Die Einweisung in die ordnungsgemäße Handhabung aktiver nichtimplantierbarer Medizinprodukte ist in geeigneter Form zu dokumentieren.
(4) Miteinander verbundene Medizinprodukte sowie mit Zubehör einschließlich Software oder mit anderen Gegenständen verbundene Medizinprodukte dürfen nur betrieben und angewendet werden, wenn sie zur Anwendung in dieser Kombination unter Berücksichtigung der Zweckbestimmung und der Sicherheit der Patienten, Anwender, Beschäftigten oder Dritten geeignet sind.
(5) Der Betreiber darf nur Personen mit dem Anwenden von Medizinprodukten beauftragen, die die in Absatz 2 genannten Voraussetzungen erfüllen und in das anzuwendende Medizinprodukt gemäß Absatz 3 eingewiesen sind.
[…]
§ 7 Instandhaltung von Medizinprodukten
[…]
(2) Der Betreiber darf mit der Instandhaltung nur Personen, Betriebe oder Einrichtungen beauftragen, die selbst oder deren Beschäftigte, die die Instandhaltung durchführen, die Voraussetzungen nach § 5 hinsichtlich der Instandhaltung des jeweiligen Medizinproduktes erfüllen.
(3) Nach der Instandhaltung nach Absatz 1 müssen die für die Sicherheit und Funktionstüchtigkeit der Medizinprodukte wesentlichen konstruktiven und funktionellen Merkmale geprüft werden, soweit sie durch die Maßnahmen beeinträchtigt werden können.
(4) Die durch den Betreiber mit den Prüfungen nach Absatz 3 beauftragten Personen, Betriebe oder Einrichtungen müssen die Voraussetzungen nach Absatz 2 erfüllen und bei der Durchführung und Auswertung der Prüfungen in ihrer fachlichen Beurteilung weisungsunabhängig sein.
§ 10 Betreiben und Anwenden von ausgewählten aktiven Medizinprodukten
(1) Der Betreiber darf ein in der Anlage 1 aufgeführtes Medizinprodukt nur betreiben, wenn zuvor der Hersteller oder eine dazu befugte Person, die im Einvernehmen mit dem Hersteller handelt,
1. dieses Medizinprodukt am Betriebsort einer Funktionsprüfung unterzogen hat und
2. die vom Betreiber beauftragte Person anhand der Gebrauchsanweisung sowie beigefügter sicherheitsbezogener Informationen und Instandhaltungshinweise in die sachgerechte Handhabung, Anwendung und den Betrieb des Medizinproduktes sowie in die zulässige Verbindung mit anderen Medizinprodukten, Gegenständen und Zubehör eingewiesen hat.
Eine Einweisung nach Nummer 2 ist nicht erforderlich, sofern diese für ein baugleiches Medizinprodukt bereits erfolgt ist.
(2) In der Anlage 1 aufgeführte Medizinprodukte dürfen nur von Personen angewendet werden, die durch den Hersteller oder durch eine nach Absatz 1 Nr. 2 vom Betreiber beauftragte Person unter Berücksichtigung der Gebrauchsanweisung in die sachgerechte Handhabung dieses Medizinproduktes eingewiesen worden sind.
(3) Die Durchführung der Funktionsprüfung nach Absatz 1 Nr. 1 und die Einweisung der vom Betreiber beauftragten Person nach Absatz 1 Nr. 2 sind zu belegen.
(4) Absatz 2 gilt nicht für in der Anlage 1 aufgeführte Medizinprodukte, die zur Anwendung durch Laien bestimmt sind. Einweisungspflichten nach anderen Vorschriften werden hiervon nicht berührt.
§ 12 Medizinproduktebuch
(1) Für die in den Anlagen 1 und 2 aufgeführten Medizinprodukte hat der Betreiber ein Medizinproduktebuch nach Absatz 2 zu führen. Satz 1 gilt nicht für elektronische Fieberthermometer als Kompaktthermometer und Blutdruckmessgeräte mit Quecksilber- oder Aneroidmanometer zur nichtinvasiven Messung.
(2) In das Medizinproduktebuch, für das alle Datenträger zulässig sind, sind folgende Angaben zu dem jeweiligen Medizinprodukt einzutragen:
1. erforderliche Angaben zur eindeutigen Identifikation des Medizinproduktes,
2. Beleg über die Funktionsprüfung und Einweisung nach § 10 Absatz 1,
3. Name der nach § 10 Absatz 1 Satz 1 Nummer 2 beauftragten Person, Zeitpunkt der Einweisung sowie Namen der eingewiesenen Personen,
4. Fristen und Datum der Durchführung sowie das Ergebnis von vorgeschriebenen sicherheits- und messtechnischen Kontrollen und Datum von Instandhaltungen sowie der Name der verantwortlichen Person oder der Firma, die diese Maßnahme durchgeführt hat,
5. Datum, Art und Folgen von Funktionsstörungen und wiederholten gleichartigen Bedienungsfehlern sowie
6. Angaben zu Vorkommnismeldungen an Behörden und Hersteller.
(3) Das Medizinproduktebuch ist so aufzubewahren, dass die Angaben dem Anwender während der Arbeitszeit zugänglich sind. Nach der Außerbetriebnahme des Medizinproduktes ist das Medizinproduktebuch noch fünf Jahre aufzubewahren.
§ 13 Bestandsverzeichnis
(1) Der Betreiber hat für alle aktiven nichtimplantierbaren Medizinprodukte der jeweiligen Betriebsstätte ein Bestandsverzeichnis zu führen. Die Aufnahme in ein Verzeichnis, das auf Grund anderer Vorschriften geführt wird, ist zulässig.
(2) In das Bestandsverzeichnis sind für jedes Medizinprodukt nach Absatz 1 folgende Angaben einzutragen:
1. Bezeichnung, Art und Typ, Loscode oder die Seriennummer, Anschaffungsjahr des Medizinproduktes,
2. Name oder Firma und die Anschrift des Herstellers oder des Bevollmächtigten oder, sofern der Hersteller keinen Unternehmenssitz in der Europäischen Union und keinen Bevollmächtigten beauftragt hat, des Importeurs,
3. die der CE-Kennzeichnung hinzugefügte Kennnummer der Benannten Stelle, soweit diese nach den Vorschriften des Medizinproduktegesetzes in der bis einschließlich 25. Mai 2021 geltenden Fassung oder nach der Verordnung (EU) 2017/745 angegeben ist,
4. soweit vorhanden, betriebliche Identifikationsnummer,
5. Standort und betriebliche Zuordnung,
6. die nach § 11 Absatz 1 Satz 2 und 3 festgelegte Frist für sicherheitstechnische Kontrollen.
[…]